RNAiとは何ですか?知っておくべきことすべて
重要なポイント:
RNA干渉(RNAi)は、RNA分子が遺伝子を沈黙させ、遺伝子の下方制御またはサイレンシングを引き起こすプロセスです。
RNAの定義
RNAはリボ核酸の略で、遺伝子発現とタンパク質合成において基本的な役割を果たす一本鎖核酸分子です。 RNA の構造は、リボース糖分子とリン酸基からなる糖リン酸骨格で構成されています。糖分子には、アデニン (A)、シトシン (C)、グアニン (G)、およびウラシル (U) の 4 種類の窒素塩基が結合しています。 RNA では、DNA にあるチミンがウラシルに置き換わります。 |  |
RNA干渉とは何ですか?
遺伝子サイレンシングは、DNA メチル化、ヒストン修飾、RNAi などのさまざまなメカニズムを通じて実現できます。 RNAi は、RNA 分子を使用して遺伝子をサイレンシングまたは分解する生物学的プロセスです。これは、遺伝子発現を、通常は転写または翻訳のレベルで阻害するプロセスです。 RNAi は、mRNA の破壊、タンパク質合成の阻害、クロマチン構造の変化など、さまざまな方法で遺伝子発現を制御します。
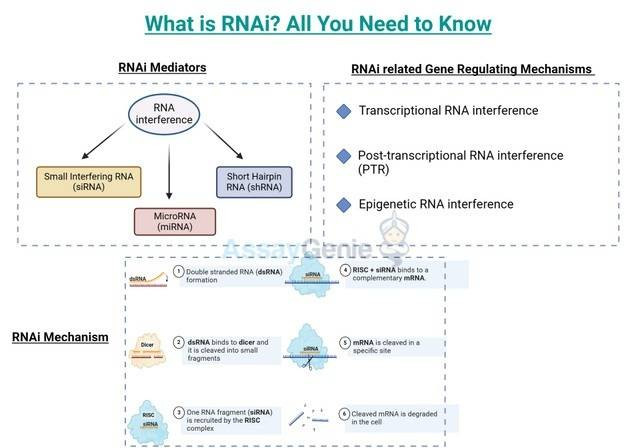
RNAi メディエーター - RNAi の種類
さまざまな形態の RNA 分子が RNA 干渉 (RNAi) を媒介し、遺伝子発現の制御において異なる役割を果たします。これらの RNA 分子はそれぞれ、転写後レベルで遺伝子発現を調節することによって RNAi 経路に寄与します。これらは、遺伝子機能、治療介入、および遺伝子調節の複雑なメカニズムを研究するための多用途のツールを提供します。
siRNA VS miRNA
特性 | siRNA | miRNA |
起源 | 外因的に導入または合成された | 外因的に導入または合成された |
構造 | 二本鎖RNA分子 | 一本鎖RNA分子 |
遺伝子サイレンシング | 特定の遺伝子を沈黙させるように設計されている | より一般的な方法で遺伝子を沈黙させる |
作用機序 | mRNAに結合して翻訳を阻害する | mRNAに結合して分解する |
ターゲットの特異性 | オフターゲット効果が少なく、より具体的 | より一般的な効果と潜在的なオフターゲット効果が発生する可能性があります |
RNA干渉はどのように作用するのでしょうか?
RNA 干渉のメカニズムは複雑で、完全には理解されていません。しかし、低分子RNAがRNAiの媒介において重要な役割を果たすことが知られている。 Small RNA は、標的 mRNA の相補配列に結合し、mRNA の分解を引き起こしたり、翻訳を妨げたりすると考えられています。

RNAi関連の遺伝子制御機構
遺伝子発現のさまざまな段階で遺伝子発現を制御できる 3 つの主なモードがあります。
RNAi干渉技術
RNA 干渉 (RNAi) テクノロジーは、遺伝子発現の選択的かつ特異的なサイレンシングを可能にする強力な遺伝ツールです。 RNAi の自然な細胞プロセスを利用して、低分子 RNA を使用して遺伝子活性を制御します。 RNAi テクノロジーには、特定のメッセンジャー RNA (mRNA) 分子を標的とする合成または内在性低分子干渉 RNA (siRNA) またはマイクロ RNA (miRNA) 分子の導入または生成が含まれます。
関連製品
 |
 |
 |
RNAi アプリケーション
遺伝子機能研究
RNAi 対 CRISPR
RNAi | CRISPR |
すべての細胞で起こる自然なプロセス | 細菌の自然メカニズムを応用した人工技術 |
可逆 | 不可逆 |
複数の遺伝子を一度に沈黙させるために使用できる | 一度に 1 つの遺伝子のみをターゲットにできる |
より具体的な | オフターゲット効果の可能性が高い |
RNAiの未来
現在、ほとんどの研究では遺伝子機能を同定するツールとして RNAi が使用されています。 RNAi を使用できる用途はこれらだけではありません。疾病管理 (ウイルス、細菌性疾患、寄生虫、遺伝性腫瘍)、商業的関心のある動物の生産、研究用の動物モデルの生産は、RNAi が使用される他の分野のほんの一部です。その他の将来の応用例としては、薬物摂取の制御、鎮痛、睡眠の調節などが挙げられます。
アッセイジーニーのブログ
Recent Posts
-
Understanding Myeloid Cell Networks in Cancer Immunotherapy
癌免疫療法における骨髄細胞ネットワークの理解免疫療法は癌治療に革命をもたらしましたが、治療後に元の免疫応答を再確立する効果は限られています。本記事では、骨髄細胞ネットワークがこのプロセスにおいて重要な …21st Aug 2025 -
PD-L1 in Cancer Immunotherapy: Insights from Recent Research
癌免疫療法におけるPD-L1:最近の研究からの洞察最近の癌免疫療法の進展は、腫瘍による免疫回避を媒介する プログラム死リガンド1 (PD-L1) の重要な役割を強調しています。本記事では、PD-L1 …21st Aug 2025 -
Role of CD25+FOXP3+CD45RA- Treg Cells in Cancer Prognosis
CD25+FOXP3+CD45RA- Treg細胞の癌予後における役割はじめに制御性T細胞(Treg細胞)は、免疫の恒常性と耐性を維持する上で重要な役割を果たすT細胞の特化したサブセットです。これらの …1st Aug 2025