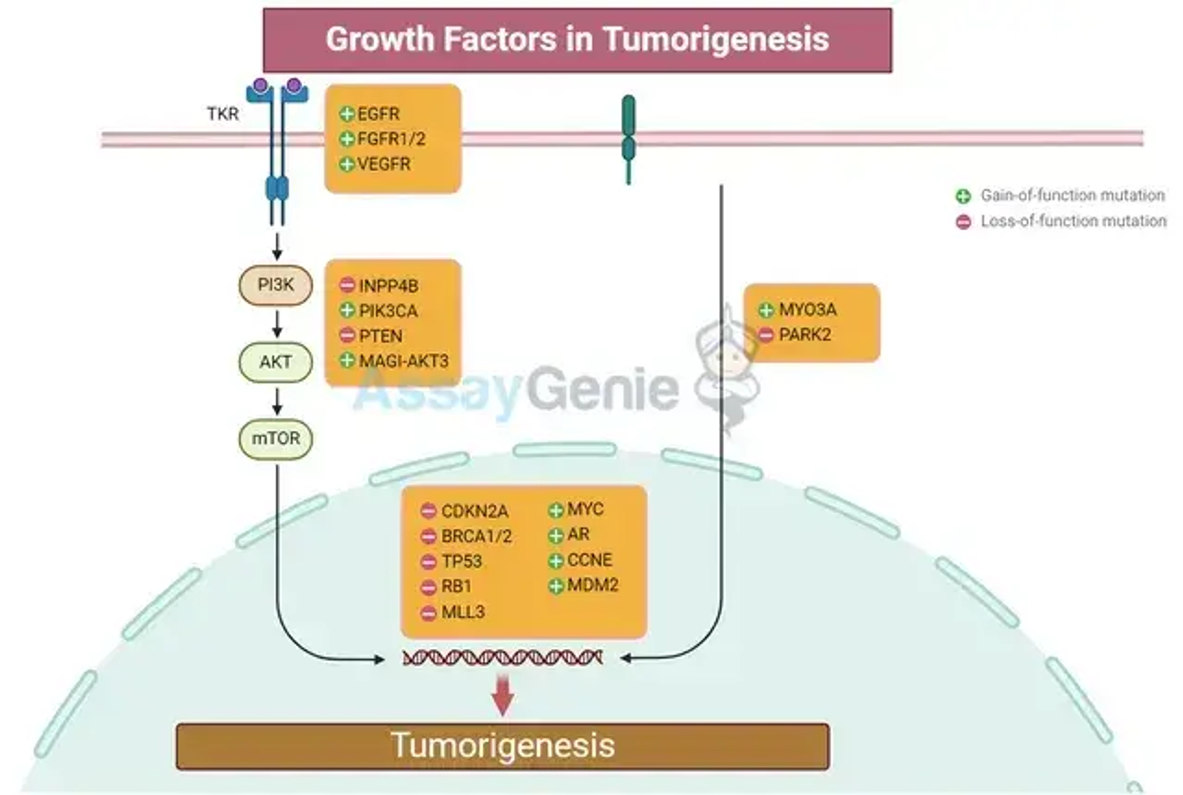
成長因子は協力して腫瘍形成を促進することができる
導入
腫瘍形成は、正常細胞が癌細胞に変化するプロセスであり、さまざまな内的および外的要因の影響を受ける多面的で複雑なイベントです。これらのうち、成長因子は細胞間のコミュニケーションと制御において極めて重要な役割を果たしており、制御が乱れると癌の発症につながる重要な要素となることがよくあります。この記事では、成長因子が複雑なネットワークと相互作用を通じてどのように協力して腫瘍形成を促進するのかを詳しく調べ、その作用の背後にあるメカニズムと癌治療への影響に焦点を当てます。
細胞調節における成長因子の役割
成長因子は、細胞表面の特定の受容体に結合するタンパク質で、細胞の成長、分化、生存、移動を調節する一連のシグナル伝達経路を誘発します。成長因子は正常な発達と組織の維持に不可欠です。しかし、成長因子の調節が乱れると、制御不能な細胞増殖やがんを引き起こす可能性があります。
腫瘍形成における主要な成長因子
成長因子間の協力のメカニズム
成長因子は単独で作用するのではなく、複雑なネットワーク内で相互作用し、腫瘍形成に相乗効果をもたらします。異なる成長因子間の協力は、いくつかのメカニズムを通じて発生します。

シグナル伝達経路間のクロストーク
腫瘍微小環境の調整
成長因子は腫瘍微小環境を再構築して腫瘍形成を促進することができます。たとえば、VEGF と FGF は協力して血管新生を促進し、成長中の腫瘍に必要な栄養素と酸素を供給します。TGF-β は免疫監視を抑制できるため、がん細胞は免疫検出を回避できます。
上皮間葉転換 (EMT) の誘導
EMT は、上皮細胞が間葉系の特性を獲得し、その可動性と侵襲性を高めるプロセスです。TGF-β や EGF などの成長因子は EMT を誘導し、腫瘍の転移を促進します。

成長因子シグナル伝達と腫瘍形成における新たな研究分野
がん研究の最近の進歩により、成長因子と腫瘍形成におけるその役割の研究に新たな側面が明らかになりました。そのような分野の 1 つが、成長因子シグナル伝達の調節におけるマイクロ RNA (miRNA) の探究です。miRNA は、転写後に遺伝子発現を調節できる小さな非コード RNA です。miRNA は、成長因子シグナル伝達経路に関与するがん遺伝子または腫瘍抑制遺伝子を標的とすることで、がんにおいて重要な役割を果たすことがわかっています。miRNA と成長因子の相互作用を理解することで、これらの調節 RNA を標的とするがん治療の新しいアプローチにつながる可能性があります。
もう 1 つの有望な分野は、がん幹細胞 (CSC) と成長因子との相互作用の研究です。CSC は、自己再生して腫瘍形成を促進する能力を持つがん細胞の小さなサブセットです。EGF や FGF などの成長因子は、CSC の特性を維持し、治療に対する耐性を促進する上で重要な役割を果たすことが知られています。 CSC における成長因子シグナル伝達経路を標的とすることで、腫瘍を根絶し再発を防ぐための新たな戦略が得られる可能性があります。
潜在的な治療ターゲット
がんの進行における成長因子の複雑な関与により、いくつかの潜在的な治療ターゲットが浮かび上がっています。
成長因子受容体: 表面に局在し、シグナル伝達において重要な役割を果たしていることから、成長因子受容体は治療の主要なターゲットです。これらの受容体を阻害するように設計されたチロシンキナーゼ阻害剤 (TKI) とモノクローナル抗体は、さまざまながんに有効であることがわかっています。
シグナル伝達中間体: PI3K/AKT/mTOR 経路など、成長因子受容体の下流のシグナル伝達経路の構成要素は、介入の追加のターゲットとなります。これらの経路を標的とする阻害剤は、がん細胞の増殖および生存シグナルを阻害することができます。
成長因子シグナル伝達の負の調節因子: チロシンキナーゼを脱リン酸化させるホスファターゼなどの負の調節因子の発現または活性を高めることは、別の治療手段となります。これらの調節因子の機能を回復すると、がん細胞における異常な成長因子シグナル伝達を弱めることができます。
ミエリンの修復
ミエリンの | ミエリンの | ミエリンの |
ミエリンの | ミエリンの | ミエリンの |
ミエリンの | ミエリンの | ミエリンの |
ミエリンの | ミエリンの | ミエリンの |
ミエリンの | ミエリンの | ミエリンの |
がん治療への影響
この表は、現在使用が承認されている最も重要な免疫チェックポイント阻害剤のいくつかを簡単に参照するためのもので、その標的の多様性と治療に使用されるがんの幅広い範囲を強調しています。
結論
がんにおける成長因子とそのシグナル伝達経路の探究は、研究と治療法開発のための豊かな環境を提供します。成長因子が腫瘍形成と治療抵抗性を促進する複雑なメカニズムを解明するにつれて、標的介入の新たな機会が生まれます。miRNA による制御からがん幹細胞集団の維持や治療抵抗性の誘発への関与まで、成長因子の多面的な役割に焦点を当てることで、研究者はがんとより効果的に闘うための革新的な戦略を考案できます。がんにおける成長因子シグナル伝達の理解から効果的な標的化までの道のりは困難を伴いますが、がん患者にとってより正確で永続的な治療を生み出す可能性を秘めています。
結論
Hanahan, D. および Weinberg, R.A.、2011。「がんの特徴:次世代」。Cell、144(5)、pp.646-674。
Lemmon, M.A. および Schlessinger, J.、2010。「受容体チロシンキナーゼによる細胞シグナル伝達」。Cell、141(7)、pp.1117-1134。
Carmeliet, P. および Jain, R.K.、2011。「血管新生の分子メカニズムと臨床応用」。Nature、473(7347)、pp.298-307。
Massagué, J.、2008。「がんにおける TGFβ」。Cell、134(2)、pp.215-230。
Weis, S.M.および Cheresh, D.A.、2011。腫瘍血管新生: 分子経路と治療ターゲット。Nature Medicine、17(11)、pp.1359-1370。
Thiery, J.P.、Acloque, H.、Huang, R.Y.J.、および Nieto, M.A.、2009。発生と疾患における上皮間葉転換。Cell、139(5)、pp.871-890。
Prenzel, N.、Fischer, O.M.、Streit, S.、Hart, S.、および Ullrich, A.、2001。細胞シグナル伝達と多様化の中心要素としての上皮成長因子受容体ファミリー。内分泌関連癌、8(1)、pp.11-31。
Ferrara, N., Hillan, K.J., Gerber, H.P., Novotny, W., 2004. がん治療のための抗VEGF抗体、ベバシズマブの発見と開発。Nature Reviews Drug Discovery、3(5)、pp.391-400。
O'Brien, J., Hayder, H., Zayed, Y., Peng, C.、2018. MicroRNAの生合成、作用機序、循環の概要。Frontiers in Endocrinology、9、p.402。
Batlle, E. and Clevers, H.、2017. がん幹細胞の再考。The New England Journal of Medicine、377(13)、pp.1250-1261。
須田 功、富澤 功、藤井 正之、2017。エルロチニブ耐性を獲得した上皮成長因子受容体変異肺癌細胞株における上皮間葉転換。Journal of Thoracic Oncology、6(7)、pp.1152-1161。
Engelman、J.A.、Zejnullahu、K.、Mitsudomi、T.、Song、Y.、Hyland、C.、Park、J.O.、Lindeman、N.、Gale、C.M.、Zhao、X.、Christensen、J.、Kosaka、T.、Holmes、A.J.、Rogers、A.M.、Cappuzzo、F.、Mok、T.、Lee、C.、Johnson、B.E.、Cantley、L.C.および Janne, P.A., 2007. MET 増幅は ERBB3 シグナル伝達を活性化することで肺癌におけるゲフィチニブ耐性につながる。Science, 316(5827), pp.1039-1043.
Polivka, J. Jr., および Janku, F., 2014. PI3K/AKT/mTOR 経路における癌治療の分子標的。Pharmacology & Therapeutics, 142(2), pp.164-175.
Sun, Y., 2010. 腫瘍微小環境と癌治療耐性。Cancer Letters, 289(2), pp.205-210.
31st Dec 2024
Recent Posts
-
Understanding Myeloid Cell Networks in Cancer Immunotherapy
癌免疫療法における骨髄細胞ネットワークの理解免疫療法は癌治療に革命をもたらしましたが、治療後に元の免疫応答を再確立する効果は限られています。本記事では、骨髄細胞ネットワークがこのプロセスにおいて重要な …21st Aug 2025 -
PD-L1 in Cancer Immunotherapy: Insights from Recent Research
癌免疫療法におけるPD-L1:最近の研究からの洞察最近の癌免疫療法の進展は、腫瘍による免疫回避を媒介する プログラム死リガンド1 (PD-L1) の重要な役割を強調しています。本記事では、PD-L1 …21st Aug 2025 -
Role of CD25+FOXP3+CD45RA- Treg Cells in Cancer Prognosis
CD25+FOXP3+CD45RA- Treg細胞の癌予後における役割はじめに制御性T細胞(Treg細胞)は、免疫の恒常性と耐性を維持する上で重要な役割を果たすT細胞の特化したサブセットです。これらの …1st Aug 2025